|
Trickreiche Transportmoleküle |
|
Meldung:
Goethe-Uni, Frankfurt |
|
|
|
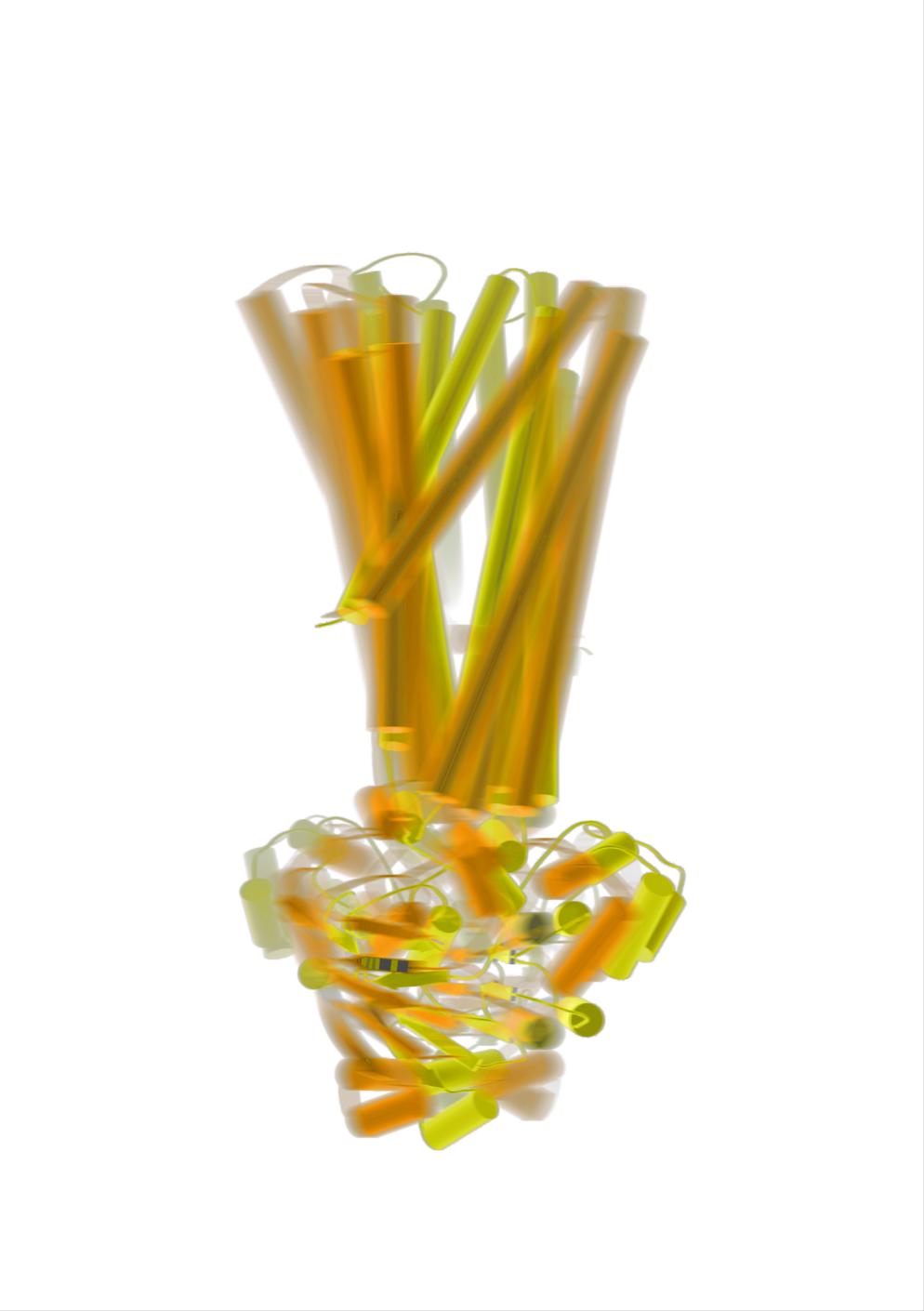 |
|
|
|
Überlagerte Momentaufnahmen
von der Schleusenfunktion eines ABC-Transporters,
aufgenommen mit Kryo-Elektronenmikroskopie.
Abb.:
Christoph Thomas & Robert Tampé (Institut für Biochemie,
Goethe Universität Frankfurt)
|
Frankfurter Forscher haben den Mechanismus eines
ABC-Transporters im Detail aufgeklärt. Fast alle Lebewesen – von
der Bakterie bis zum Menschen – beherbergen in ihren
Zellmembranen schleusenartige Proteinkomplexe, die unerwünschte
oder lebensgefährliche Moleküle hinausbefördern. Nicht immer zum
Vorteil des Menschen, denn in Bakterien oder Krebszellen sind
die sogenannten ABC-Transporter auch verantwortlich für
Resistenzen gegenüber Antibiotika oder Chemotherapie. Nun ist es
Forschern der Goethe-Universität zusammen mit Kollegen des
Frankfurter Max Planck-Instituts für Biophysik gelungen, den
Transportmechanismus in allen Stadien zu entschlüsseln.
In den vergangenen fünf Jahren hat die Gruppe von Prof. Robert
Tampé vom Institut für Biochemie der Goethe-Universität intensiv
daran gearbeitet, Proben empfindlicher Membranprotein-Komplexe
so präparieren, dass man sie mit Kryo-Elektronenmikroskopie
untersuchen kann. Die Kryo-Elektronenmikroskopie liefert
hochaufgelöste Bilder, weil sie Moleküle einfriert, so dass
Unschärfen durch Bewegungen minimiert werden.
Will man komplexe Molekülen wie ABC-Transporter nicht nur scharf
abbilden, sondern ihnen auch bei der Arbeit zuschauen, braucht
man Momentaufnahmen verschiedener Stadien. Die Biochemiker um
Tampé konnten diese Stadien gezielt herbeiführen, indem sie den
Transporter mit unterschiedlichen Konzentrationen von ATP und
ADP versorgten. Der Transporter benötigt diese Energie, um
Moleküle gegen das Konzentrationsgefälle zwischen dem
Zellinneren und seiner Umgebung zu befördern.
In der aktuellen Ausgabe der Fachzeitschrift Nature zeigen Tampé
und seine Kollegen aus der Biophysik acht hochaufgelöste
Konformationen eines ABC-Export-Komplexes, der aus zwei
verschiedenen Proteinuntereinheiten besteht. Erstmals konnten
die Forscher auch Zwischenstadien des Transportprozesses
sichtbar machen. Die Herausgeber von Nature haben diese
bedeutsame Entdeckung als Titelgeschichte der aktuellen Ausgabe
ausgewählt.
„Die Arbeit könnte zu einem Paradigmenwechsel in der
Strukturbiologie führen, da alle Bewegungszustände einer
zellulären Maschine in fast atomarer Auflösung aufgeklärt werden
konnten“, erklärt Prof. Robert Tampé. „Aufgrund dieser
unerwarteten Entdeckung können wir bisher kontrovers diskutierte
Fragen zum Transportmechanismus der ABC-Transporter beantworten,
die von besonderer medizinischer Bedeutung sind.“ Darüber hinaus
konnten die Forscher erstmals beobachten, wie sich die Schleusen
nach außen oder innen öffnen. Die Auflösung von 2,8 Angström
(Zehnmillionstel eines Millimeters) ist die höchste Auflösung,
mit der je eine ABC-Transporter-Struktur mithilfe der
Kryo-Elektronenmikroskopie abgebildet wurde.
Publikation:
Susanne Hofmann, Dovile Januliene, Ahmad R. Mehdipour, Christoph
Thomas, Erich Stefan, Stefan Brüchert, Benedikt T. Kuhn, Eric R.
Geertsma, Gerhard Hummer, Robert Tampé, Arne Moeller:
Conformation space of a heterodimeric ABC exporter under
turnover conditions, in Nature, 17. Juli 2019. DOI:
10.1038/s41586-019-1391-0
|