|
Wandel für die Wiederverwertung - Einblicke in das
Ribosom-Recycling |
|
Meldung:
Goethe-Uni, Frankfurt |
|
|
|
 |
|
|
|
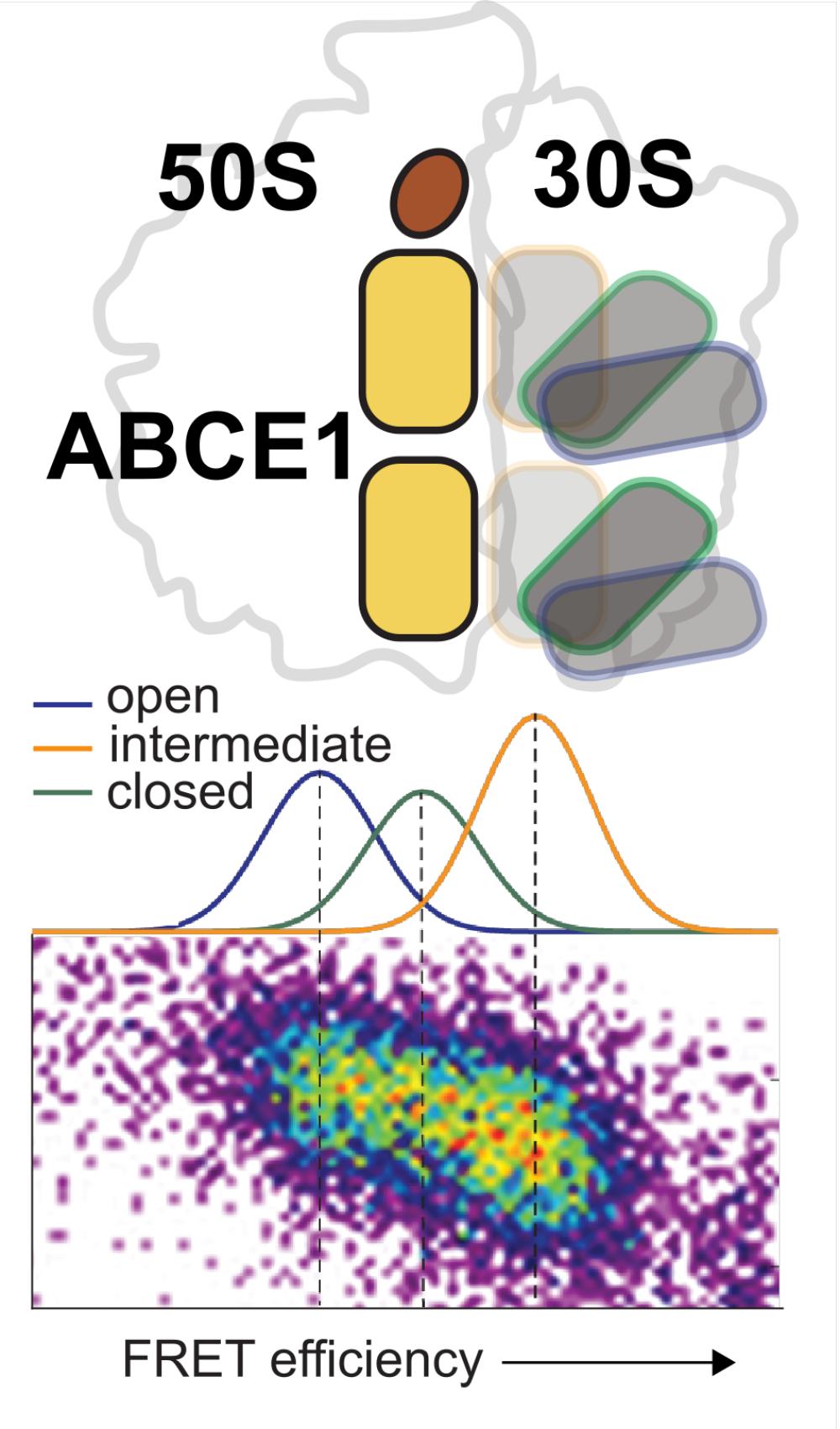
Drei
Zustände der Nukleotidbindedomänen sind im Histogramm zu
erkennen: offen, intermediär und geschlossen. Bild: T.
Cordes, LMU München
|
Ribosomen sind molekulare Maschinen, die in der
Zelle Proteine erzeugen. Nach getaner Arbeit müssen Ribosome
wieder funktionstüchtig gemacht werden. Dieser Prozess ist
entscheidend für die Qualitätskontrolle der erzeugten Proteine
und somit für die gesamte Zell-Homöostase und
entwicklungsbiologische Prozesse. Biochemiker der Goethe
Universität und Biophysiker der LMU München haben nun einem der
entscheidenden Enzyme für die Ribosmon-Wiederverwertung, ABCE1,
bei der Arbeit zugeschaut und gezeigt, dass es strukturell
unerwartet wandelbar ist.
An
Ribosomen wird die genetische Information von der Boten-RNA
abgelesen und in Proteine übersetzt. Wenn sie ein Protein
erzeugt haben, aber auch, wenn fehlerhafte Proteine im Ribosom
steckenbleiben, müssen die Ribosomen „recycelt“ werden, so dass
sie für eine neue Syntheserunde funktionsfähig sind. In allen
Organismen (außer in Bakterien) koordiniert das Enzym ABCE1
diesen Vorgang, bei dem die Ribosomen in ihre beiden
Untereinheiten zerlegt werden. Der Biochemiker Robert Tampé und
der LMU-Biophysiker Thorben Cordes haben in Kooperation mit
Wissenschaftlern der Universität Groningen (Niederlande)
gezeigt, dass ABCE1 drei räumliche Konformationen einnimmt, um
das Recycling voranzutreiben. Über ihre Ergebnisse berichten die
Wissenschaftler in der aktuellen Ausgabe des Fachmagazins Cell
Reports.
Das
Enzym ABCE1 kann ATP, die Energiewährung der Zelle, spalten und
die dabei gewonnene Energie zur Trennung der beiden
Ribosomen-Untereinheiten nutzen. „Jüngste strukturelle und
funktionelle Daten haben gezeigt, dass dabei ein
Konformationswechsel des Enzyms, also eine Änderung seiner
räumlichen Struktur, für die vielfältigen Funktionen von ABCE1
unerlässlich ist“, sagt Cordes. Sein Team hat nun mit einem
integrierten Versuchsansatz – unter anderem mithilfe der
sogenannten Einzelmolekül-FRET-Methode – die Formvariabilität
von ABCE1 auf der Ebene einzelner Molekülebene direkt
beobachtet.
Dabei stellten die Wissenschaftler fest, dass die beiden
ATP-Bindestellen von ABCE1 drei Konformationen einnehmen können,
die sich in einem dynamischen Gleichgewicht befinden: offen,
intermediär und geschlossen. Die Interaktion von ABCE1 mit dem
Ribosom und das zur Verfügung stehende ATP beeinflussen die
strukturelle Dynamik beider ATP-Stellen. So entsteht ein
komplexes Netzwerk unterschiedlicher Zustände, wobei Ribosom und
ATP das Gleichgewicht in Richtung der geschlossenen Formen
verschieben.
„Wir gehen davon aus, dass die Konformationen funktionell
unterschiedliche Rollen bei der Ribosomenspaltung, aber auch für
die anderen vielfältigen Funktionen von ABCE1 haben“, sagt
Cordes. „Das Ribosom-Recycling wird von einer außergewöhnlich
komplexen und konservierten Maschinerie mit bisher ungeahnter
medizinischer Bedeutung dirigiert“ ergänzt Robert Tampé.
Publikation:
Giorgos Gouridis, Bianca Hetzert, Kristin Kiosze-Becker, Marijn
de Boer, Holger Heinemann, Elina Nürenberg-Goloub, Thorben
Cordes, Robert Tampé:
ACBE1 controls ribosome recycling by an asymmetric dynamic
conformational equilibrium, in: Cell Reports 2019 DOI:
10.1016/j.celrep.2019.06.052
https://doi.org/10.1016/j.celrep.2019.06.052
|